多囊卵巢综合征
多囊卵巢综合征(PCOS),是一种以高雄、排卵障碍以及卵巢多囊样改变为特征的疾病。其病因未明,以对症处理和经验性治疗为主。PCOS可能导致严重的代谢异常后遗症,如使糖尿病与心血管疾病风险增加,而这些因素在PCOS的长程治疗中均需予以考虑。本文的宗旨在于考察现有的最佳依据用于PCOS的临床诊疗。
背景
发病率、定义以及诊断标准
目前并没有一个被普遍认可的PCOS定义。近年来,有关PCOS诊断标准的专家意见层出不穷(表1)。鹿特丹标准,取代了美国国立卫生研究院(NIH)的诊断标准(1),将卵巢的超声学检查证据纳入其中(2),而PCOS的超声诊断标准由专家共识决定(框1)(3)。这些诊断标准将较多的轻症表型的患者纳入其中,被认为增加了PCOS的普遍性,使治疗复杂化。美国雄激素学会(AES)将雄激素增多症作为必要条件,结合其他症状做出诊断(4)。雄激素增多症可由临床检查(如多毛或痤疮)或血清激素检测确定,而所有的诊断策略都需要首先排除其他导致高雄的原因(如成年型先天性肾上腺增生症,高泌乳素血症以及雄激素分泌肿瘤)。所有的诊断标准均包括一种以上的症状或体征(表1,框3)。例如,单一的卵巢多囊样改变是一种非特异表现,并常见于不存在任何内分泌或代谢异常的女性。胰岛素抵抗总是见于PCOS女性,特别是存在雄激素增多症的患者,然而却没有被纳入任何一个诊断标准(5)。
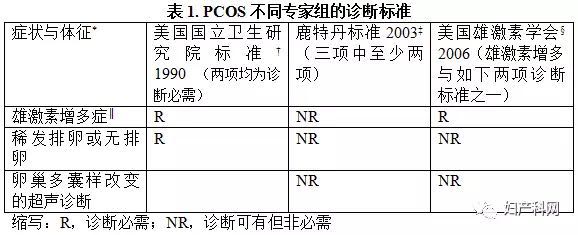


根据不同的诊断标准,PCOS的发生率有所不同。慢性高雄激素无排卵(NIH诊断标准)的女性约占生育年龄妇女的7%。多毛症或外周血雄激素水平增高在白种与黑种人女性中的发生率无显著差异(6)。较为宽泛的鹿特丹标准较NIH标准,使正常促性腺激素无排卵的PCOS发病率由55%升高至91%(7)。而采用AES标准诊断的PCOS发生率介于上述两者之间(4)。
病因
导致PCOS的遗传因素仍不清楚,缺少可推荐的基因筛查项目,而环境因素也尚未明确。胰岛素抵抗可能是导致该综合征发生的主要环节(5)。合并肥胖可能放大PCOS的疾病效应。然而,肥胖并不是PCOS的诊断标准之一,并且20%的PCOS患者不存在肥胖。肥胖在美国的发生率高于其他国家,因此PCOS的表型可能有所不同。代偿性高胰岛素血症可能导致性激素结合蛋白(SHBG)水平降低,因此,循环中具有生物学活性的雄激素水平升高,而后者可刺激肾上腺与卵巢合成更多的雄激素。胰岛素对下丘脑还具有直接效应,例如异常激活食欲与促性腺激素的释放。雄激素增多症,也是该综合征发生的主要环节,可能具有多种病因,而其中一些与胰岛素抵抗无关。
所有的诊断标准均需要排除其他导致相似症状和体征的疾病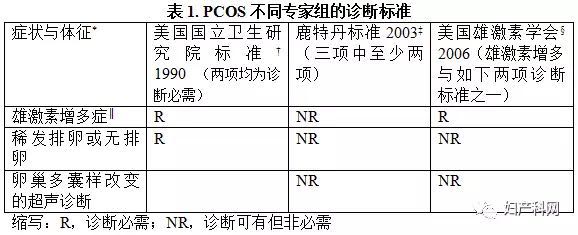
Dunaif A, Givens JR, Haseltine FP, Merriam GR, editors. Polycystic ovary syndrome. Boston (MA): Blackwell Scientific Publications;1992.
Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome. Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group. Fertil Steril 2004;81:19–25.
Azziz R, Carmina E, Dewailly D, Diamantl-Kandarakis E, Escobar-Morreale HF, Futterwelt W, et al. Positions statement: criteria for defining polycystic ovary syndrome as a predominantly hyperandrogenic syndrome: an Androgen Excess Society guideline.Androgen Excess Society. J Clin Endocrinol Metab 2006;91:4237–45.
雄激素增多症可表现为多毛症或生化检测雄激素增多。
临床表现
PCOS的女性患者常见月经紊乱(从闭经到月经过多)与不孕。因此,对PCOS患者进行卵巢刺激的风险倍受关注,因为这些患者是发生卵巢过度刺激综合征和多胎妊娠的高风险人群。此外,PCOS患者发生妊娠期并发症的风险增加,包括妊娠期糖尿病以及妊娠期高血压疾病等(8)。而助孕治疗所导致的医源性多胎妊娠将大大增加妊娠期并发症的风险。
皮肤疾病在PCOS患者中较为常见,特别是由于雄激素过多导致的多毛与痤疮,以及较为轻度的男型脱发(9)。PCOS患者发生胰岛素抵抗及其相关异常的风险增加,如代谢综合征(框2)(10),非酒精性脂肪肝(11),以及肥胖相关异常,如睡眠呼吸暂停(12)。反之,所有上述异常均是远期代谢异常后遗症的危险因素,如2型糖尿病与心血管系统疾病。PCOS女性患者还存在子宫内膜癌的多种危险因素,包括慢性无排卵、向心性肥胖以及糖尿病,尽管其与PCOS相关性仍存有争议(13)。近年来,PCOS患者情绪障碍和抑郁的关系正逐渐受到关注(14)。

PCOS的鉴别诊断
PCOS的鉴别诊断涉及其他导致雄激素过多的原因(框3)。诊断所需的关键病史采集与体格检查内容列举在(框1)。病史采集时应关注雄激素过多相关体征的出现以及过程、月经史以及用药史,包括外源性雄激素的使用等。糖尿病以及心血管疾病(特别是一级亲属中出现早发型心血管疾病[男性小于55岁和女性小于65岁])家族史十分重要。


体格检查应评估脱发、痤疮、阴蒂增大以及体毛分布,并进行盆腔检查评估卵巢大小。应明确记录是否存在痤疮及其严重程度。应记录胰岛素抵抗的相关体征,如高血压、肥胖、向心性肥胖以及黑棘皮症。黑棘皮症表现为皮肤呈现天鹅绒样、苔藓样、乳头瘤样以及色素沉着。可见于颈后、腋窝、乳房下方,甚至是外阴。黑棘皮症的出现更多的是胰岛素抵抗或药物反应的一种体征,而不仅仅是一种病症。应考虑到其他与黑棘皮症相关的病理状态,如胰岛素瘤与一些恶性疾病,特别是胃腺癌。阴蒂增大鲜少与PCOS存在相关性,若出现应考虑排除其他疾病。
由于Cushing综合征极其罕见(1/1,000,000),而相关筛查试验的灵敏度和特异性达不到100%(15),不推荐对所有慢性雄激素增高无排卵的女性常规进行Cushing综合征的筛查。对于同时存在Cushing综合征表现的患者,包括满月脸、水牛背、腹纹、向心性肥胖或高血压,应接受筛查(见框1)。近端肌病与易发瘀斑并不是PCOS患者的典型表现,也提示可能存在Cushing综合征。

卵巢或肾上腺的雄激素分泌肿瘤也伴随外周血雄激素水平增高。然而,缺乏一个确切的数值用以诊断肿瘤,因为缺乏排除肿瘤的最低雄激素水平。以往,当睾酮水平大于2ng/mL和硫酸脱氢表雄酮(DHEAS)水平超过700mg/dL时,怀疑分别存在卵巢肿瘤和肾上腺疾病,但是相关界定值的特异性和灵敏度很低(16)。
针对不明原因雄激素增多的最佳循环血雄激素检测方法并不确定。当前AES推荐采用平衡透析法直接检测或基于准确的总睾酮(采用柱层析法进行放射性免疫测定,或通过质谱检测)以及SHBG(如采用竞争结合法或高质量基于免疫的测定方法)检测值计算游离睾酮浓度。因为缺乏标准的睾酮检测方法,所有临床医师都应该熟悉本院实验室的分析性能与正常参考范围,而女性体内睾酮水平灵敏度与可信度很低(17)。DHEAS水平对发生快速男性化的病例可能有帮助(肾上腺来源的标记),但在普通多毛症的评估方面存在争议。
女性体内的雄激素来源于肾上腺与卵巢。肾上腺主要合成雄激素活性较弱的脱氢表雄酮(DHEA)或DHEAS(90%为肾上腺来源)。这些激素与雄烯二酮都是活性更强雄激素(如睾酮或二氢睾酮)的前体。卵巢是睾酮的主要来源,大约75%循环血中的睾酮源于卵巢(主要通过激素前体在周围组织转化而来,包括肝脏、脂肪、皮肤等组织,也通过直接分泌)。雄烯二酮,主要来源于卵巢,是唯一一种在绝经前女性体内水平高于男性的循环雄激素,然而其雄激素活性仅有睾酮的10%。二氢睾酮是活性最强的雄激素,然而其在循环血中含量极低,主要通过细胞内5-α还原酶作用于睾酮而产生。
泌乳素的轻度升高在PCOS患者比较常见(18)。泌乳素水平可以反映泌乳素瘤的存在,后者可分泌大量的泌乳素并可刺激卵巢合成雄激素,但极少导致慢性高雄激素性无排卵。考虑到其复杂的临床表现以及频繁出现甲状腺疾病,血清促甲状腺激素水平升高在月经失调的女性较有意义。
临床考虑与推荐
谁需要接受非典型先天性肾上腺增生症的筛查?如何筛查?
非典型先天性肾上腺增生症,常被称为迟发型先天性肾上腺增生症,可见于无排卵和多毛症的成年女性,绝大多数病例无一例外的由类固醇合成酶,21羟化酶(CYP21)编码基因缺陷导致。在欧洲与美国,先天性肾上腺增生症最高发于德系犹太人(Ashkenazi Jews),其次是西班牙人、南斯拉夫人、美洲阿拉斯加印第安人、因纽特人以及意大利人(19)。高发地区的女性患者在疑似诊断PCOS时应对17-羟孕酮水平进行筛查。
针对CYP21突变所导致的非典型先天性肾上腺增生症进行筛查时,应在清晨空腹检测17羟孕酮的水平。若检测值低于2ng/mL则判为是正常。若是在卵泡期的上午进行检测,一些研究者认为应该将参考界限定在4ng/mL(20)。如果是在黄体期检测将使其检测特异性降低。若检测到17羟孕酮水平升高,应进行肾上腺皮质激素(ACTH)兴奋试验。
肥胖症PCOS患者,减重是否可以改善卵巢功能?
肥胖症是导致PCOS女性患者生殖与代谢异常的重要原因。多项研究表明,减重可以通过降低循环雄激素水平以及重新建立月经周期,改善PCOS患者代谢综合征的基本指标。体重减轻可以提高妊娠率,减轻多毛症,并改善糖脂代谢(21-24)。研究表明,应用减肥药物如奥利司他(一种脂肪吸收的肠道抑制剂)以及西布曲明(一种食欲抑制制剂)均可以改善PCOS患者卵巢功能(25,26)。PCOS患者病态肥胖者行胃分流术后,其生殖与代谢异常均趋于正常(27)。上述好转均见于减轻原有体重5%的患者(28)。体重减轻后游离睾酮水平的降低可能与SHBG水平升高有关(28)。在正常体重PCOS患者中,减轻体重的作用未知。
PCOS是否增加2型糖尿病的风险?谁需要接受筛查?
诊断为PCOS的患者,应对空腹及75g糖餐后2h的血糖进行检测以筛查2型糖尿病及糖耐量异常(29)(框1)。回顾性研究表明,PCOS女性患糖尿病的风险较对照人群增加2-5倍(30,31)。在一项前瞻性队列研究中,11.9%年龄大于30岁的PCOS患者被诊断为2型糖尿病,而对照人群中仅1.4%(32)。另一项队列研究显示,采用WHO不太严格的诊断标准(2h血糖大于等于140mg/dL),40%的美国PCOS女性存在糖耐量异常(33,34),而在体重偏小的欧洲人群中发生率稍低(35)。大约3-10%的PCOS患者存在未经确诊的糖尿病。PCOS患者发生糖耐量异常的危险因子——年龄、高体重指数(BMI)、腰臀比过大以及糖尿病家族史——与其他人群相同。

缺乏胰岛素抵抗的筛查实验,而代谢综合征越来越受人认识,这是一种增加糖尿病与心血管疾病风险的胰岛素抵抗的临床表型(框2)。代谢综合征在PCOS女性中十分常见,一项大样本的多中心研究显示33%的患者存在异常(10)。

空腹血糖水平预测PCOS患者糖耐量异常的效用很低,因此,一些专家组建议增加口服糖耐量试验来筛查代谢综合征。糖尿病预防计划以及其他糖尿病预防研究结果显示,生活方式干预与降糖药物(如二甲双胍)均可显著降低糖耐量异常女性患者发展为糖尿病的风险(36)。
对PCOS患者常规检测胰岛素的意义不大。胰岛素检测水平并不能提示患者对治疗的反应性。
PCOS患者是否存在发生心血管疾病的远期风险?谁应该接受筛查?
通过了解BMI、空腹血脂与脂蛋白以及代谢综合征危险因素,对PCOS患者心血管疾病风险进行筛查(见框2和框3),并定期复查,因为每年高达20%的PCOS患者发展为糖耐量减退(37),不过低密度脂蛋白(LDL)水平基本不发生改变(38)。规律的锻炼与体重控制被证实可以降低心血管疾病发病率与死亡率。在使用药物前应首先考虑生活方式的调整。


血脂异常在PCOS患者是较为常见的代谢异常。根据全美胆固醇教育计划指南,PCOS患者中大约70%存在临界或高血脂(39),其中低密度脂蛋白水平不成比例的升高(38,39)。
尽管PCOS被高度怀疑可能增加心血管系统疾病的发生风险及早发风险,但相关文献依据不足,缺乏PCOS患者心血管疾病发生风险增加的前瞻性研究。然而一些队列研究(包括护士健康研究)提示,在未绝经期人群中,若早年PCOS的症状越多或月经稀发越频繁,心血管疾病的发生风险越高(41,42)。研究显示,绝经期PCOS女性亚临床动脉粥样硬化的发生率较对照人群升高(发生率由低于10%的PCOS合并颈动脉中层增厚到40%PCOS女性合并冠状动脉钙化)(43-45)。
无妊娠需求的PCOS患者,什么是治疗月经紊乱最好的用药方法?
联合激素类避孕药
PCOS月经紊乱的治疗有几种选择。联合低剂量激素类避孕药是月经紊乱最常使用的长程治疗方法,并被推荐为一线治疗方法。 尽管缺乏针对PCOS女性的高质量研究,总体来说,联合激素类避孕药可以通过不同的机制使患者受益,包括抑制垂体黄体生成素的分泌,抑制卵巢雄激素的分泌,以及升高循环血SHBG的水平。个体化治疗可能涉及不同的剂量及联合用药方式,因此相关风险收益比也不尽相同。比方说,不同的孕酮制剂对循环血SHBG水平存在不同的影响(46),但其临床有效性却不明确。目前缺乏足够的证据提示何种联合激素避孕药对PCOS患者月经紊乱最为有效。
孕激素
缺乏使用长效和间断口服醋酸甲羟孕酮治疗多毛症的研究。周期性口服孕激素或黄体酮节育器预防子宫内膜癌最为有效,但对PCOS患者的作用未知。孕激素类避孕药或黄体酮节育器是保护子宫内膜的选择用药,但与50-89%的异常子宫出血相关。
胰岛素增敏剂
原本研发用于治疗2型糖尿病的药物同样用于治疗PCOS。起初大多数研究主要关注增加外周组织胰岛素敏感性、降低循环血胰岛素水平的药物。这些药物包括双胍类(如二甲双胍)和噻唑烷二酮类(如吡格列酮与罗格列酮)(48,49)。这些药物鲜少导致低血糖。上述药物属胰岛素增敏剂,但是每种药物效用及风险收益比各不相同。药物种类之间存在差异,比如双胍类可以减轻体重而噻唑烷二酮类可能增加体重。同类的不同药物之间的风险收益比也可能存在显著差异(50)。由于导致体重增加,噻唑烷二酮类已较少用于PCOS的治疗。尽管如此,采用上述药物提高胰岛素敏感性可以降低循环血雄激素水平,改善排卵与糖耐量(51,52)。
由于治疗可以改善排卵率,如何选择避孕方式十分重要。胰岛素增敏与降低雄激素的药物效果不容易区分,因为胰岛素敏感性的一点点改善就可以升高SHBG从而减少生物活性雄激素的水平。
现有的降糖药物都没有被年美国食品与药品管理局(FDA)批准用于PCOS相关的月经紊乱,尽管二甲双胍的风险收益比提示其安全性最佳。缺乏在患有PCOS的妇女、儿童或成人中使用上述药物一年或以上的随机对照研究。这些药物对在预防PCOS患者子宫内膜增生过长或肿瘤形成中的作用仍鲜为人知。
无妊娠需求PCOS患者,降低心血管疾病与糖尿病风险最好的用药方法是什么?
生活方式调整是改善心血管疾病与糖尿病的最佳方法。胰岛素增敏剂与抑制素也可用于治疗。
生活方式调整
加强锻炼与饮食调整与药物相比,对于降低糖尿病风险有过之而无不及(36)。体重减轻可以改善PCOS相关的代谢异常。就体重减轻而言,能量限制是关键,而不是饮食结构调整(53),一些小型的研究显示特定的低能量饮食对PCOS女性并无其他益处(54)。因此,对于PCOS女性,除了能量限制,并没有理想的饮食调整方法。
胰岛素增敏剂
糖尿病预防计划显示,二甲双胍可减缓高危人群(如糖耐量减低的患者)向糖尿病方向发展(36),类似的结果也见于其他降糖药物对高危个体的治疗中。在使用二甲双胍治疗的PCOS患者中,糖耐量得到改善或长期稳定(55)。二甲双胍可能与体重减轻有关,但结果并不一致(52)。二甲双胍通常联合生活方式调整用于治疗PCOS。近来研究提示在改善生活方式的基础上,使用二甲双胍所带来的益处十分有限(56,57)。
二甲双胍导致乳酸酸中毒的风险较小,大多发生在糖尿病控制不好和肾功能受损的患者。胃肠道症状(腹泻、恶心、呕吐、腹胀、胃胀以及厌食)是最常见的不良反应,可以从服用小剂量开始,然后逐渐增加用量,或者选用缓释制剂。PCOS患者最常用的剂量为每日1,500-2,000mg,分几次服用。
目前有关胰岛素增敏剂预防PCOS患者发生糖尿病的数据有限。然而,有关糖尿病预防的研究结果可能使糖耐量异常或代谢综合征的处理更为积极,以预防糖尿病的发生。
抑制素
另一篇文献记载有益于心血管与内分泌的治疗是采用抑制素(58)。然而该药物对PCOS年轻女性,特别是成年女性预防心血管疾病的远期效应暂未可知。
联合激素避孕药与孕激素
没有证据显示联合激素避孕药与孕激素会增加PCOS患者糖尿病与心血管疾病的风险,因此这些药物可考虑用于治疗。在普通人群中,激素类避孕药与2型糖尿病的发生风险并无相关性(59)。激素类避孕药并不增加PCOS患者糖尿病的风险,尽管这些药物通常对胰岛素的敏感性存在不良影响且呈剂量依赖性(60,61)。因此,低剂量激素类避孕药被推荐。口服避孕药可能与循环血甘油三酯和高密度脂蛋白(HDL)水平升高相关,但不会随用药时间延长而加重(62)。没有证据显示口服避孕药治疗的PCOS患者较普通人群心血管事件发生率增加,尽管将一些不良事件的危险因素考虑在内,如高血压、肥胖、血栓形成病史与吸烟。单独使用孕激素的代谢危险因素尚不明确。
对于有妊娠计划的PCOS患者,什么是有效的诱发排卵方案?
没有关于PCOS患者如何初次以及随后选择诱发排卵的循证医学证据。美国生殖医学协会与欧洲人类生殖与胚胎协会(ASRM/ESHRE)建议,在任何干预开始之前,应该在孕前咨询中强调生活方式改变(特别是超重患者减轻体重与锻炼)、戒烟以及戒酒(63)。
抗刺激素药物克罗米芬曾经一度是诱发排卵的一线用药。然而,近来的随机对照研究与Cochrane系统回顾的结果显示,芳香化酶抑制剂,来曲唑,其排卵率、临床妊娠率以及活产率高于克罗米芬(64,65)。如果使用克罗米芬或来曲唑无法使患者成功妊娠,二线治疗的选择是外源性促性腺激素,或腹腔镜下卵巢手术(63)。
所有促排卵药物均可能导致多胎妊娠以及相关的产科与新生儿风险(如早产和妊娠高血压疾病)。克罗米芬与来曲唑导致双胎妊娠的风险相当(64)。相关事件的发生率在接受促排卵治疗的PCOS中甚至更高(63)。
芳香化酶抑制剂
芳香化酶抑制剂如来曲唑,超说明书用于诱发排卵的一线与二线治疗。在一项早期的纳入了4项研究包含662名PCOS患者的meta分析中,使用克罗米芬与来曲唑的妊娠率相当(RR:1.02;95%CI,0.83-1.26)(66)。然而,在一个更新的随机对照研究中,来曲唑较克罗米芬更为有效,活产率更高(27.5% vs 10.1%, P=0.007)且累计排卵率更高(61.7% vs 48.3%, P<0.001)(64)。系统回顾证据支持来曲唑较克罗米芬具有较高的活产率(OR,1.64;CI,1.32-2.04)与临床妊娠率(OR,1.40;CI,1.18-1.65)(65)。因此,对于PCOS女性患者,由于来曲唑的活产率高于克罗米芬,应作为一线促排卵药物。
当使用来曲唑促排卵,应告知患者来曲唑不同于克罗米芬,尚未取得FDA批准。与克罗米芬相同,来曲唑也禁用于妊娠期妇女。开具来曲唑的处方时,起始剂量是从自然月经或孕激素诱发月经的第3、4或5天开始,每天2.5mg连续使用5天。如果诱发排卵失败,则增加剂量至每天5mg连用5天,最高可达7.5mg/天。剂量超过7.5mg/天时,可能导致与使用克罗米芬类似的内膜菲薄(67)。
克罗米芬
克罗米芬是惯用于无排卵女性(包括PCOS患者)的一线用药,而几项多中心随机对照研究中,与单用二甲双胍或安慰剂相比,支持使用克罗米芬作为一线用药。对于不同人群,半年活产率为20%-40%(68-70)。半数女性使用50mg克罗米芬可以获得妊娠,另有20%女性使用100mg可以获得妊娠(71)。大多数患者在最初的六个促排周期中可以获得妊娠,稳定的月妊娠率提示延长药物治疗时间可能会带来持续的益处(69)。克罗米芬禁用于妊娠期妇女。
现已发展了不同的克罗米芬用法,包括延长使用时间(72),口服避孕药预处理(73)以及添加地塞米松。地塞米松是使用克罗米芬的附加用药,可以增加克罗米芬抵抗的PCOS患者排卵与妊娠率(74)。
促性腺激素
促性腺激素通常用于克罗米芬促排卵失败的PCOS患者。低剂量促性腺激素可提高单卵泡发育与排卵的概率,以及较低的卵巢过度刺激综合征的风险(75)。在PCOS患者推荐使用低剂量的促性腺激素(63)。
卵巢打孔术
腹腔镜下激光或电凝卵巢打孔对无排卵的亚临床不孕与PCOS患者作为一线治疗的价值不确切(76),通常被推荐为二线处理方法。无论是激光还是电凝打孔都没有显著的益处,并且在改善排卵与妊娠率方面与使用促排卵激素作为二线治疗方法相比没有显著差异(76)。经腹腔镜下卵巢打孔术后,患者的多胎妊娠率降低。在一些病例中,卵巢打孔仅能暂时改善生育力,而后续使用克罗米芬或促性腺激素促排仍十分必要(77)。腹腔镜下卵巢打孔的远期效应并不清楚,但无法改善PCOS患者的代谢异常(78)。
胰岛素增敏剂
二甲双胍
随机对照研究结果并不支持单用二甲双胍作为治疗不孕症的一线用药。使用克罗米芬的活产率是二甲双胍的三倍。Meta分析结果显示使用二甲双胍时添加克罗米芬较单用克罗米芬可以提高妊娠率,特别是在肥胖的PCOS患者(OR,2.67;95%CI,1.45-4.94)(79)。二甲双胍对人胚胎没有致畸或致死作用,是妊娠期的安全用药(妊娠期B类用药)。没有确凿的证据显示妊娠早期使用二甲双胍可以预防流产。一项随机研究中,若在验孕阳性时停用药物,使用二甲双胍与克罗米芬的流产率相当。
不同药物对PCOS患者多毛症的治疗效果如何?
尽管医学干预可以改善多毛症,但尚未能完全满足患者的需求,而且通常是治标不治本。激光治疗在临床中的应用逐渐增多。总体来说,联合治疗较单一治疗的效果更好。除了有关盐酸依氟鸟氨酸乳膏的研究,多毛症的临床研究多为小样本、单中心,且对临床疗效与患者反应的评价不全面。因此,PCOS患者多毛症的一线治疗不确切。
联合激素类避孕药
没有联合激素类避孕药得到FDA的批准用于治疗多毛症。一些观察性或非随机的研究指出,口服避孕药可以改善PCOS患者的多毛症,但是缺乏可以提供有力证据的研究(80)。少有研究比较不同种类的联合激素类避孕药的治疗结局,而且没有一种药在治疗PCOS多毛症方面存在优势。一些研究发现口服避孕药与其他药物联用可能更有益,最常见的是与螺内酯联用。如果联合激素类避孕药中含有屈螺酮成分,则应该减少螺内酯的剂量并评估患者的钾离子水平。
抗雄激素制剂
没有针对雄激素增高症研发的抗雄激素制剂,或相关制剂并未获得FDA的批准用于降低雄激素。这些药物都是经验性地用于PCOS患者。多毛症的相关研究质量不佳。近期一项meta分析从348项合格的研究中仅纳入了12项(81),结果显示相关制剂的作用甚微。这些复合物首先拮抗睾酮或其他雄激素与受体的结合。拮抗雄激素可以改善其他代谢指标,如体脂比例与循环血脂水平(82)。所有这些制剂都存在一些益处,但PCOS患者多毛症的最佳选择仍不清楚。作为一类药物,雄激素拮抗剂具有致畸性,具有导致妊娠期男性胚胎外生殖器女性化的风险(两性畸形)。因此,这类药物通常需与口服避孕药联用。
螺内酯
螺内酯,一种利尿剂与醛固酮拮抗剂,可以拮抗剂的形式与雄激素受体结合,还具有其他的药理机制,包括抑制卵巢与肾上腺类固醇激素合成,在毛囊中竞争结合雄激素受体,以及直接抑制5α还原酶活性。常用剂量为每次25-100mg,每天两次,采用滴定法确定药物剂量,以最大程度发挥药物作用并避免如直立性低血压的副作用。通常需要六个月或以上的时间达到临床效果。大约20%的女性在使用螺内酯后出现月经频发(83)。由于可能导致并加重高血钾,螺内酯应慎用于肾功能减退的妇女。妊娠期用药导致男性胎儿两性畸形的情况较为罕见。
氟他胺
氟他胺,一种雄激素受体激动剂,一些小样本研究显示,该药是另一种对多毛症有效的非甾类雄激素拮抗剂。最常见的药物副作用包括皮肤干燥,罕见的情况有药物性肝炎。常用剂量为125-250mg/d。该药物的致畸性十分显著,使用期间应该避孕。氟他胺还与生活方式调整和二甲双胍等联用于PCOS的治疗,可能具有叠加效应(82)。
非那司提
非那司提可以抑制两种类型的5α还原酶(第一类,主要表达于皮肤;第二类,主要表达于前列腺与生殖系统组织)。治疗前列腺癌的制剂为5mg片剂,而治疗男型秃发使用1mg片剂。非那司提与其他雄激素拮抗剂相比耐受性更好,肝肾毒性小;然而已明确该药物对男性胎儿存在致畸作用,应使用足量的避孕药避孕。
胰岛素增敏剂
有关二甲双胍用于治疗多毛症有效性的研究数据很少(80)。在一项持续44周的胰岛素增敏剂研究中,仅在曲格列酮(噻唑烷二酮现已从市场下架)的最高剂量下对PCOS患者多毛症有轻微改善(51)。需要更为精确和长程的研究比较不同种类胰岛素增敏剂的异同及其远期效益。目前,使用胰岛素增敏剂的有效性甚微而且也不十分明确(84)。
依氟鸟氨酸
时下热门的依氟鸟氨酸已获得FDA批准用于治疗女性面部多毛。用药6个月后,大约60%的女性有所改善,1/3临床治愈。治愈率不受年龄以及既往除毛处理的影响,在白种人中的治愈率高于其他人种(37% vs 22%),对黑种人无效。使用方法是每天两次涂擦于面部。副作用主要表现为局部的刺痛、灼热、红斑,以及罕见皮疹(85)。
辅助化妆对多毛症的处理有效吗?
机械性地除毛(刮毛、拔毛、用蜡脱毛、脱毛霜、电除毛以及激光蒸发)通常是女性的首选。没有证据显示刮毛会增加毛囊的密度或增粗毛发直径。在忍受范围内,拔毛可能较为有效,但应小心避免毛囊炎、色素沉着和瘢痕形成。
有关激光治疗的研究较电除毛更为正规,前者是PCOS患者去除多余毛发有效的方法(86)。激光去除毛发的机制在于,毛囊黑素细胞可以吸收激光波长的光,后者可以选择性的以热量破坏靶位点而不影响周围组织。肤色浅与毛色深的女性患者更适宜选用这种处理方法,并且在毛发生长周期使用最为有效。由于不同的毛囊处在毛发生长周期的不同阶段,因此重复治疗十分必要(87)。对雄激素过高的患者,推荐同时辅以药物处理以降低雄激素水平,否则在雄激素的作用下,新的毫毛将会分化为终毛而导致多毛的复发。在激光治疗的基础上添加依氟鸟氨酸,较单用激光治疗更为有效(88)。
推荐总结与结论
以下的推荐与结论都是基于良好和一致的科学证据(A级):
增加运动量结合饮食调整对于降低糖尿病风险,与药物治疗相比有过之而无不及。
使用胰岛素增敏剂增加胰岛素敏感性,与循环血雄激素水平降低、排卵率以及糖耐量改善有关。
应将来曲唑作为PCOS女性患者促排卵一线用药,较克罗米芬的活产率较高。
在激光治疗基础上添加依氟鸟氨酸,较单用激光对多毛症的治疗更为有效。
以下的推荐与结论都是基于有限的和不甚一致的科学证据(B级):
诊断为PCOS的患者进行空腹以及75g糖餐后血糖检测,以筛查是否存在2型糖尿病和糖耐量异常。
对PCOS患者进行BMI、空腹血脂、载脂蛋白水平以及代谢综合征危险因素的检测,以筛查是否存在心血管疾病风险。
减轻体重可以改善妊娠率,减轻多毛症,并改善糖耐量与血脂水平。
在使用二甲双胍的基础上使用克罗米芬可能提高妊娠率,特别是对肥胖的PCOS患者。
如果使用克罗米芬或来曲唑无法获得妊娠,推荐使用外源性促性腺激素或腹腔镜卵巢手术作为二线治疗。
以下的推荐与结论都是基于专家意见和共识(C级):
联合低剂量激素类避孕药用于长期治疗月经紊乱,并且是治疗的首选。
非典型先天性肾上腺增生症高危患者,或疑似诊断为PCOS患者,应接受17羟孕酮的筛查。
PCOS患者可以使用低剂量促性腺激素进行促排。
PCOS患者多毛症的首选治疗方法不明确。
翻译:华芮 南方医科大学南方医院
审校:张师前 山东大学齐鲁医院
文章来源:OBSTETRICS & GYNECOLOGY,VOL .131,No.6,JUNE2018